Американські дослідники розробили маскуючу систему для бактерій, що дозволяє їм тимчасово ховатися від імунної системи людини. Бактерії, покриті особливою оболонкою, здатні знаходити ракові пухлини і, розмножуючись в них, виробляти протипухлинні токсини.

Використання бактерій для терапії – новий, альтернативний і багато в чому спірний підхід до лікування широкого спектру видів раку. Одна з найбільш очевидних проблем цього методу лікування – токсичність бактерій-доставників для організму людини. На відміну від багатьох традиційних способів цільової доставки ліків, бактерії продовжують жити і розмножуватися в організмі пацієнта.
Імунна система людини розпізнає бактерії як чужорідні і небезпечні, що викликає запальну реакцію. Цю проблему вирішують або генною інженерією бактерій для зачистки поверхні мікроорганізмів від антигенів, на які реагує імунна система, або покриттям поверхні живих доставщиків ліків в спеціальну молекулярну захист.
Перший спосіб послаблює бактерії: вони погано розмножуються і швидко гинуть, так і не доставивши ліки. Другий здатний дати мікроорганізмам занадто багато часу для розмноження, що призведе до неконтрольованого зростання і через що може початися сильна запальна реакція.
Тому в новому дослідженні, результати якого опубліковані в журналі Nature Biotechnology, американські біотехнологи зосередилися на генній інженерії та керованому біосинтезі молекулярного захисту в бактеріях Escherichia coli Nissle 1917. Вони використовували синтезований самими бактеріями капсульний полісахарид (CAP), що покриває їх поверхню і захищає від виявлення імунною системою людини, і знайшли спосіб контролювати його виробництво.
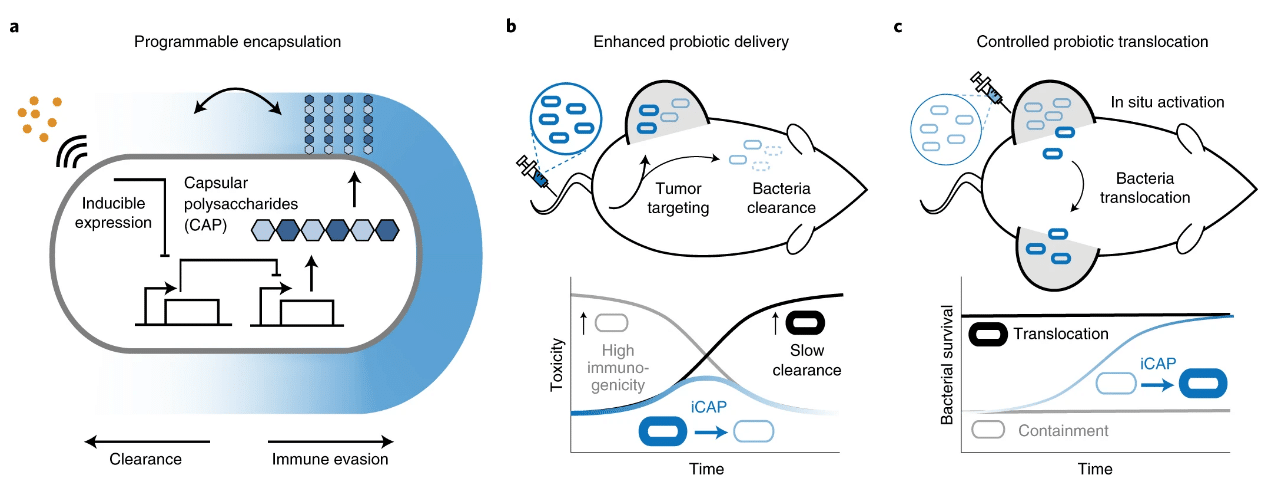
«Ми зламали систему CАР пробіотичного штаму E. coli Nissle 1917 — пояснює Тецухіро Харімото (Tetsuhiro Harimoto), аспірант кафедри біомедичної інженерії в Колумбійському університеті (США) і співавтор дослідження. – З CAP ці бактерії можуть тимчасово ухилятися від імунної атаки; без CAP вони втрачають свій захист і можуть виводитися з організму. Тому ми вирішили спробувати створити ефективний вимикач”.
Для цього дослідники розробили систему iCAP (індукований CAP). Вони контролюють систему iCAP, використовуючи зовнішній сигнал – невелику молекулу, що називається IPTG (ізопропіл-B-D-тіогалактопіранозид). У присутності IPTG бактерія синтезує CAP і створює собі плащ-невидимку, що приховує її від імунної системи. Якщо цю молекулу прибрати, то протягом шести годин захисний покрив з бактерій повністю спаде.
«Що дійсно цікаво в нашій роботі, так це те, що ми можемо динамічно управляти системою, — коментує Тал Даніно (Tal Danino), доцент кафедри біомедичної інженерії Колумбійського університету і один з наукових керівників дослідження. – Ми здатні регулювати час, протягом якого бактерії виживають в крові людини, і збільшувати максимально переносиму дозу бактерій. Ми також показали, що наша система відкриває нову стратегію доставки бактерій, в якій можна вводити бактерії в одну відому пухлину і змушувати їх контрольовано мігрувати в віддалені пухлини, такі як метастази — ракові клітини, які поширюються в Інші частини тіла».
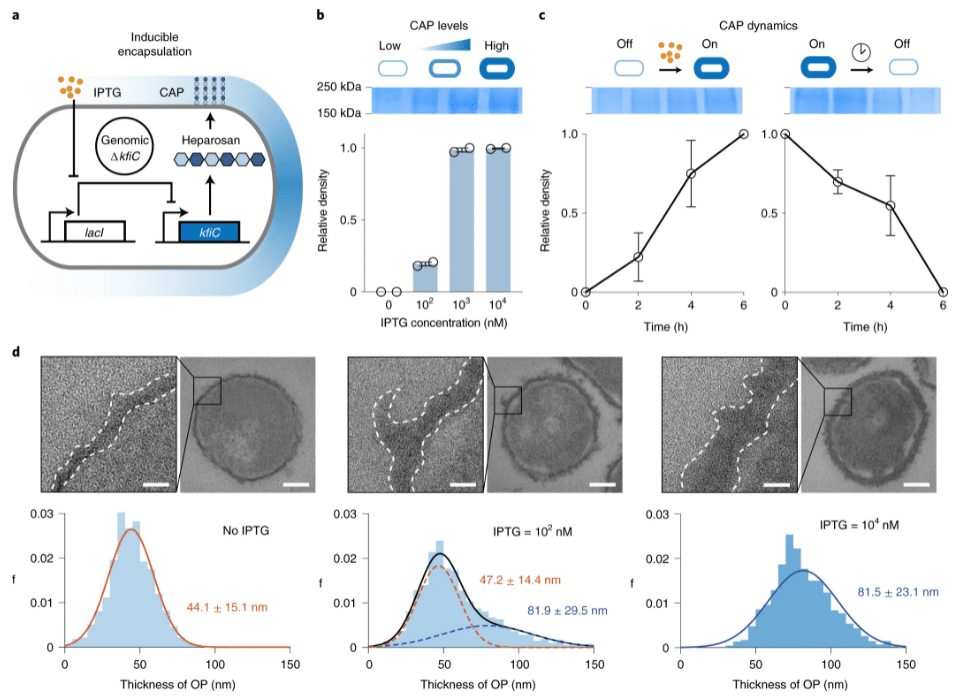
Перевірку ефективності системи iCAP проводили на мишах, хворих на рак. Дослідники додали в E. coli з системою iCAP можливість виробництва протипухлинного токсину і змогли зменшити зростання пухлини в моделях раку кишечника і раку молочної залози у гризунів. Причому результати для E. coli з системою iCAP були значно кращими, ніж без неї.
Команда також продемонструвала контрольовану міграцію бактерій в організмі до пухлинних метастазів. Вони вводили E. coli з системою iCAP в одну пухлину, давали мишам воду, що містить IPTG, ніж активували CAP захист. Після цього спостерігали, як iCAP E. coli виходять з початкової пухлини і мігрують в неін’єційовані пухлини.
Надалі автори планують вдосконалювати свою технологію, використовуючи інші організми, типи молекулярних покривів (на зразок CAP) і системи управління з можливістю автономної роботи поверхневих властивостей терапевтичних бактерій. Крім того, одна з головних і найбільш складних майбутніх завдань — клінічні випробування системи на людині, більш чутливому до бактеріальних ендотоксинів в порівнянні з мишами.
