Нещодавно виявлена ще одна передбачувана мутація, яка веде до раннього старіння, — в гені nsd1. Відомо вже кілька десятків таких генів. Гіпотетично блокування цих ділянок геному могла б уповільнити старіння і продовжити життя. Але втручання в геном здатне привести і до інших неприємних наслідків. Втім, вчених це не зупиняє. Досліди по відключенню генів старіння проводяться зараз відразу в декількох лабораторіях.

Молоді люди похилого віку
Перша публікація про передбачуваний ген старіння з’явилася в 1996 році в журнал Science. Її автори, вчені з Японії і США, вивчали людей з синдромом Вернера — при цьому захворюванні організм зношується в два рази швидше, ніж зазвичай, і людина в сорок років виглядає на вісімдесят. Дослідники звернули увагу на мутацію в гені WRN, розташованому на восьмій хромосомі. Припустили, що з-за неї порушуються якісь важливі процеси в організмі, і це прискорює старіння.
Через кілька років гіпотеза частково підтвердилася. Синдром Вернера дійсно страждають тільки ті, у кого є дві копії мутованого гена WRN. Проте його навряд чи можна вважати геном старіння в прямому сенсі: це посередник, який впливає на інші ділянки ДНК.
Річ у тім, що WRN виробляє білок, який підтримує структуру і цілісність людської ДНК. Будь-які його дефекти (а вони неминучі, якщо в цьому гені є мутація) змінюють механізми реплікації і відновлення пошкодженої молекули. Це, в свою чергу, позначається на роботі інших ділянок генома, у тому числі пов’язаних зі старінням.
Старше своїх років
Під підозру потрапив ген меланокортинового рецептора першого типу (MC1R), відкритий нещодавно нідерландськими, британськими і китайськими вченими. Вони співвіднесли геноми 2693 літніх людей з зовнішніми проявами віку, відображеним на їх світлинах.
Проаналізувавши більше восьми мільйонів одно нуклеотидних поліморфізмів — відмінностей в послідовності ДНК розміром всього в один нуклеотид, встановили: ті, що знаходяться в гені MC1R, пов’язані зі зовнішніми ознаками старіння. Так, люди з двома копіями мутантного варіанта MC1R виглядають в середньому на два роки старші фактичного віку.
Два роки — начебто небагато. Однак якщо носії мутації курять, занадто часто відвідують солярій і ведуть не надто здоровий спосіб життя, то розрив між видимим і реальним віком збільшується, попереджають автори дослідження.
Схожим чином діє і мутантний варіант гена nsd1. За даними канадських і британських вчених, ті, хто отримав її копії від кожного з батьків, старіють швидше за ровесників.
Заразне старіння
У процесах старіння грає помітну роль також ген CD36, виявлений в минулому році американськими генетиками. Судячи з усього, він відповідає за припинення поділу клітини, що сигналізує про її швидку загибель.
Досліджуючи зістарені клітини, вчені звернули увагу на незвичайну активність CD36. Щоб вивчити її детальніше, провели два експерименти. У першому модифікували 15 відсотків молодих здорових клітин в культурі, що ген CD36 працював ефективніше. В результаті ті перестали ділитися і виявляли явні ознаки старіння. Більш того, заразили цим інші клітини у культурі з нормальним геном.
У другому досліді генетики деякий час протримали в поживному розчині культуру зістарених клітин, потім замість неї помістили більш молоді клітини. Ті, в свою чергу, раптово припинили ділитися, немов перейнявши якості колишніх “мешканців”. Це підтверджують експерименти на фібробластах шкіри і легенів. Але чому так відбувається, незрозуміло, визнають автори дослідження.
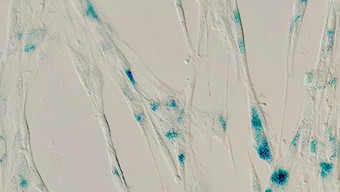
Зістарені клітини під мікроскопом: синім кольором позначені області підвищеної експресії гена CD36
Ген відключив, молодість продовжив
Швейцарські вчені експериментують з геном PUM2. В молодих клітинах вироблений ними білок необхідний для синтезу пептидів. А от у більш літніх він перетворюється на серйозну перешкоду: його молекули збивається в клубки і заважають РНК передавати інструкції з ядра в ті частини клітини, де збираються білки.
Так, одна з “жертв” PUM2 — речовина MFF, важлива для утилізації пошкоджених мітохондрій. Річ у тому, що вміст цих клітинних енергостанцій, за винятком АТФ і продуктів життєдіяльності, ніколи не покидає їх меж. Коли ж мітохондрії зношуються, в них утворюються своєрідні “дірки”, через які в цитоплазму клітини просочуються агресивні молекули, що пошкоджують ДНК клітини і викликають перебої в її роботі. Молоді клітини справляються з такими аваріями, в тому числі завдяки MFF, розщеплюючи мітохондрії на частини і переварюючи пошкоджені фрагменти. У літніх клітинах цьому перешкоджає PUM2. У результаті клітини старіють швидше і гинуть.
Якщо ж PUM2 вчасно відключити або вирізати з ДНК, старіння сповільниться, припустили вчені і заблокували цей ген у черв’яків-нематод. Мітохондрії у всіх клітинах помолодшали, а тварини прожили значно довше, ніж їх немодифіковані побратими. А ось з мишами цей прийом виявився не настільки ефективний. Мітохондрії помолодшали тільки в клітинах кишківника.
На черзі — досліди з культурами людських клітин. Дослідники сподіваються знайти більш безпечний спосіб скоротити кількість білка, виробленого PUM2, не редагуючи геном.
