Міжнародна група вчених виявила механізм, що дозволяє стовбуровим клітинам приймати рішення про долю дочірніх клітин ще під час поділу. Отримані дані допоможуть в розробці нових способів стимулювання регенерації тканин для прискорення відновлення після пошкоджень, а можливо, і для лікування дегенеративних захворювань.
Тканинні стовбурові клітини містяться у великій кількості тканин нашого організму. Вони відповідають за регенерацію цих тканин і можуть стати будь-якою клітиною, характерною для конкретної тканини, в якій вона знаходиться. Це властивість називається мультипотентністью, на відміну від плюрипотентності ембріональних стовбурових клітин, які можуть стати будь — якою клітиною всього організму – хоч нейроном, хоч міоцитом (клітиною м’язової тканини).
При розподілі стовбурової клітини утворюються дві дочірні, які можуть бути як стовбуровими, так і диференційованими клітинами тканини. Нова робота дослідників з Університету Гельсінкі (Фінляндія), а також їх колег зі Швеції та Німеччини присвячена вивченню механізму, згідно з яким дочірні стовбурові клітини визначають, диференціюватися їм або ж залишитися стовбуровими. Точніше, на долю дочірніх клітин впливає нерівномірне успадкування мітохондрій від батьківської клітини.
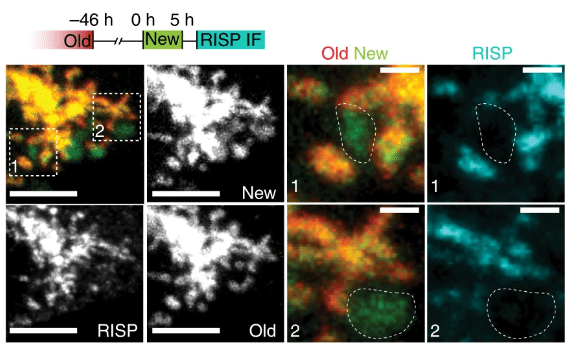
При вивченні поділу епітеліальних стовбурових клітин вчені виявили, що якщо в дочірню клітину потрапляє досить багато старих, але при цьому більш активних мітохондрій, вона втрачає здатність до самооновлення і диференціюється в клітину, що підтримує функцію епітелію. Водночас інша дочірня клітина, яка отримала молодші мітохондрії, продовжує жити як стовбурова.
- Вчені знайшли ще одну причину пермського вимирання
- Виявлено дивний вплив стояння у пробці на серцево-судинну систему
Вся річ у тім, що в недавно синтезованих мітохондріях низький рівень особливого залізо-сірчаного білка, що бере участь в ланцюзі перенесення електронів — важливому етапі клітинного дихання. Через це в органелах глюкоза більшою мірою окислюється по альтернативному (щодо стандартного гліколізу) пентозофосфатному шляху, що дозволяє дочірній клітині залишатися стовбуровою. У другій клітині більш зрілі мітохондрії в повну силу використовують звичайний гліколіз для окислення глюкози і отримання енергії, що сприяє диференціюванню клітини.
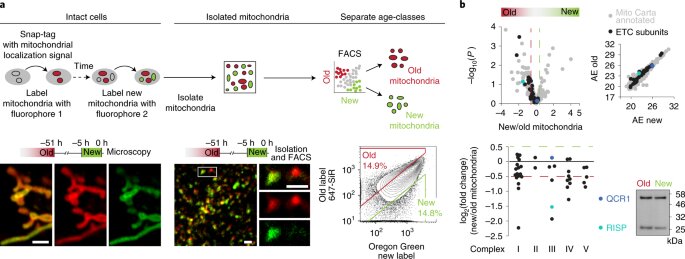
“Включення генів, що визначають клітинні функції, в підсумку визначає і диференціювання клітин, але метаболізм, мабуть, служить найпершим фактором, що впливає на їх долі», – коментує роботу доцент Пекка Катайісто (Pekka Katajisto) з Гельсінського інституту природничих наук (HiLIFE) Гельсінського університету.
«Коли ми обмежили клітинне дихання, зменшивши кількість одного білка, який у великій кількості міститься в старих мітохондріях, дочірні клітини фактично залишилися самооновлюваними стовбуровими клітинами”, – додає доктор-дослідник Джулія Говеніус (Julia Govenius) з Гельсінського університету.
Їх робота наочно демонструє, що навіть невеликі відмінності в білковому складі мітохондрій можуть впливати на метаболізм цілих клітин і в підсумку на долю цих клітин в тканинах. Це відкриття – частина фундаментального дослідження, яке закладає основу для розробки нових способів стимулювання регенерації тканин (наприклад, при дегенеративних захворюваннях) або для прискорення відновлення після їх пошкодження.
Стаття з результатами дослідження опублікована в журналі Nature Cell Biology.
