Білки риб, що мешкають біля дна океану під великим тиском, виявилися захищені молекулами триметиламіноксиду. Ця сполука добре зв’язує воду і не дозволяє біологічним молекулам втрачати правильну тривимірну форму і руйнуватися.

Ліпарова риба Notoliparis kermadecensis, знята на глибині семи кілометрів / © PNAS
Біосфера Землі простягається від багатокілометрової висоти в атмосфері, де можна виявити лише бактерії, до найглибших частин Світового океану, населених специфічними тваринами. Крім цього, окремі мікроби освоїли товщу гірських порід на великій відстані від поверхні.
Ці жителі прикордонних областей біосфери змушені пристосовуватися до екстремальних умов, в яких інші організми довго не протягнуть. Їх так і називають – екстремофіли: наприклад, термофіли виносять дуже високу температуру, кріофіли — навпаки, низьку, а барофіли, або п’єзофіли, пристосовані до проживання в умовах високого тиску.
Такі риби та інші тварини, що мешкають на багатокілометровій глибині в океані. Їх можна виявити навіть в найглибшій його частині — в Маріанській западині, на відстані більше 11 кілометрів від поверхні. Це химерні створіння, які набули в процесі еволюції специфічні адаптації до життя під тиском в 1,1 кілобара, або понад тисячу атмосфер. Подібні зміни зачіпають і морфологію мешканців глибин, і їх поведінку, і навіть функціонування їх білків.
Тому дослідники з Великобританії, автори нової статті в журналі Communication Chemistry, вирішили розібратися з адаптаціями глибоководних риб на молекулярному рівні.
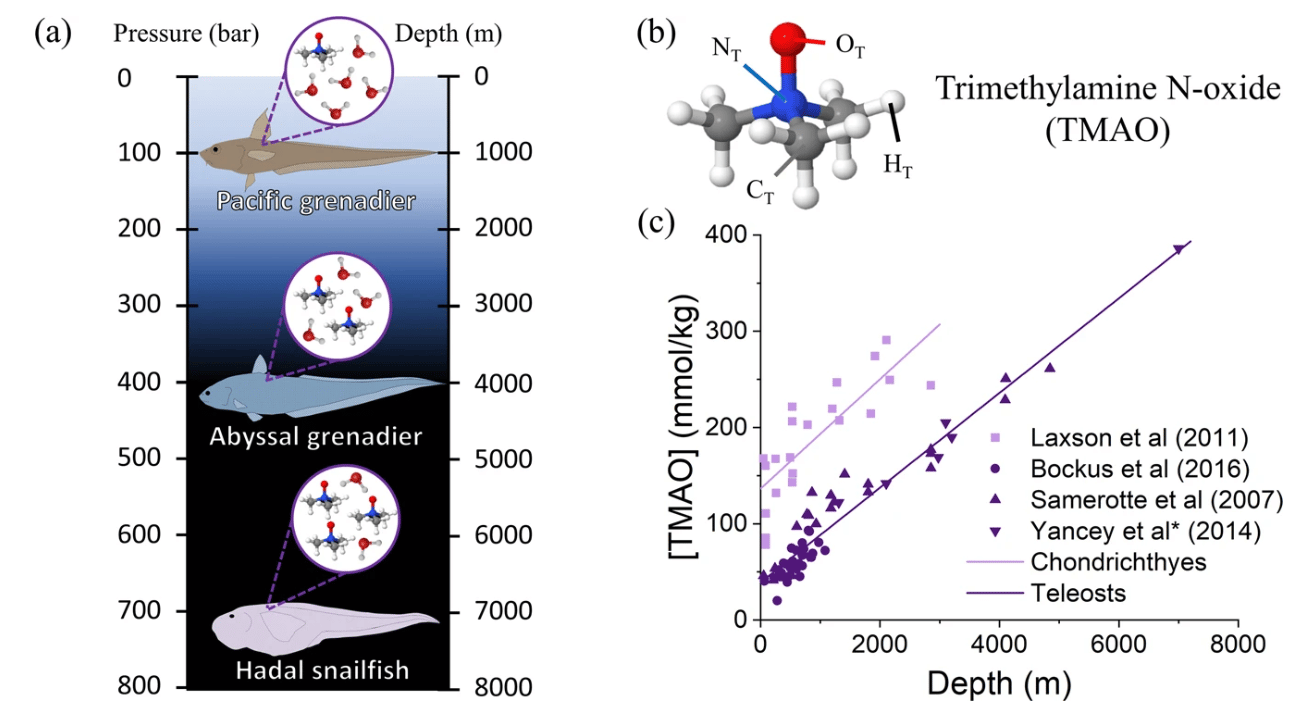
Вміст ТМАО в тканинах риб на різній глибині і структура його молекули / © Laurent, H. et al.
Вчені відзначають, що при екстремальних значеннях тиску у морських жителів виникають проблеми з їх біологічними молекулами. Вони починають втрачати стабільність, що спершу призводить до невеликої втрати в обсязі (компактизації молекул) — приблизно на один відсоток. При тиску два кілобари білки гірше олігомерізуются, тобто повільніше утворюють агрегати, що складаються з декількох молекул. Потім при тиску в чотири кілобари білки починають денатурувати – втрачати правильну тривимірну форму, визначену амінокислотною послідовністю і необхідної для їх роботи. В результаті у внутрішні порожнини білкових молекул потрапляє все більше води, що “не передбачено” в конструкції біомолекул і здорово їх псує.
- Всього пара келихів вина в тиждень скорочують обсяг мозку
- Світлотерапія зменшить побічні ефекти від лікування раку
- Кесарів розтин знизив силу імунної відповіді дітей на вакцинацію
Щоб уберегти свої білки від цих небажаних процесів, барофіли синтезують особливі молекули — п’єзоліти. Це розчинні у вигляді сполуки, здатні до стиснення, такі як триметиламіноксид, або триметиламін N-оксид (ТМАО).
Молекули TMAO оточують білки і зв’язують воду на їх поверхні. Автори статті досліджували цей процес за допомогою методу нейтронного розсіювання та комп’ютерного моделювання молекул.
Виявилося, особливо підходяща для зв’язування води структура ТМАО утворює безліч водневих зв’язків завдяки своїй несучуму заряду частині — нітрозогрупи. Це робить воду, що оточують білки, більш впорядкованою, а її молекули — менш рухливими. В результаті розчин і занурені в неї білки менше змінюються при зростанні тиску до екстремальних значень.
Вчені також відзначили, що вміст ТМАО в тканинах різних риб тим вище, чим глибше вони живуть.
